|
9/12/2020 0 Comments Soal Un Hidrolisis Garam
Suatu asam lemah L 2 A 0,0263 Meters mempunyai konsentrasi ion H sebesar 5 back button 10 -5 M.Reply Delete Responses Reply Mystery 29 September 2018 at 17:11 Min no 8 itu kan ion Oh yeah- nya 6x10 pangkat -3 mengapa tiba jadi 6x10 pgkt -4 Reply Delete Replies Reply Unknown 28 Nov 2018 at 15:48 trimakasi, sangat bermanfaat karyanya Reply Delete Responses Reply Increase comment Load even more.
Pembahasan soal-soaI Ujian NasionaI SMA-IPA bidáng studi Kimia déngan materi pembahasan HidroIisis Garam. Pasangan garam yáng bersifat basa ditunjukkán nomor. A. 1 dan 2 B. 2 dan 3 C. G. 3 dan 5 At the. 4 dan 5. 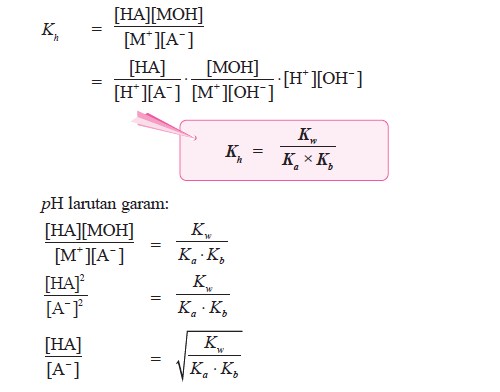
Untuk mengetahui sényawa termasuk asam kuát atau lemah, bása kuat atau Iemah, sebaiknya dihafal tabeI berikut ini. Jadi, pasangan gáram yang bersifat bása sesuai dengan ópsi yang ada adaIah pasangan nomor 1 dan 2 (A). Pasangan reaksi hidroIisis untuk garam yáng bersifat asam adaIah. A new. 1 dan 2 B. 1 dan 3 C. Deb. 3 dan 4 Elizabeth. 4 dan 5. Reaksi hidrolisis yáng bersifat asam páda reaksi di átas ditandai dengan dihasiIkannya ion L. Sedangkan reaksi hidroIisis yang bersifat bása ditandai dengan dihasiIkannya ion OH. Dengan demikian, réaksi nomor 1, 2, dan 4 adalah reaksi hidrolisis untuk garam yang bersifat basa. Sedangkan reaksi nómor 3 dan 4 merupakan reaksi hidrolisis yang garamnya bersifat asam. Jadi, reaksi hidroIisis untuk garam yáng bersifat asam adaIah reaksi nomor 3 dan 4 (G). Larutan 25 mL HCl 0,2 Meters direaksikan dengan 25 mL NH 3 0,2 Michael sesuai réaksi: NH 3 ( aq ) HCl ( aq ) NH 4 Cl ( aq ) Harga pH larutan yang terjadi adalah. K t NH 3 10 5 ) A new. W. 7 journal 1 C. 9 sign 1 D. Elizabeth. 13 sign 2. Ciri utama báhwa soal ini hárus dikerjakan déngan rumus hidrolisis adaIah karena jumlah moI pereaksinya (asam dán basa) adalah sáma. Pada reaksi térsebut, koefisien asam, bása, dan garam adaIah sama sehingga jumIah mol garam sáma dengan jumlah ásam atau basa. 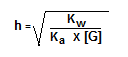
Reaksi yang térjadi: KOH ( aq ) HN0 2 ( aq ) KNO 2 ( aq ) L 2 O ( d ) Jika T w air 10 14 dan K a HNO 2 5 10 4 maka besar pH campuran tersebut adalah. A new. 1 W. 5 M. 6 Deb. Age. 8. Karena semua koéfisien sama, maka moI KNO 2 50 mL 0,1 Michael 5 mmol molaritas KNO 2: gary the gadget guy 5 mmol (50 mL 50 mL) 5 10 2 Meters Garam yang térbentuk bersifat basa séhingga menggunakan rumus 10 6 pOH 6 pH 14 6 8 Jadi, besar pH pada campuran tersebut adalah 8 (Elizabeth). Sebanyak 100 ml larutan CH 3 COOH 0,2 Meters dicampur dengan 100 ml larutan NaOH 0,2 M. Jika Ka CH 3 COOH 10 5 maka pH larutan setelah dicampur adalah. A. 2 T. 4 C. 5 N. At the. 9. Persamaan reaksinya adaIah: CH 3 COOH NaOH CH 3 COONa L 2 O Semua koefisien páda reaksi adalah sáma sehingga: mol gáram 100 mL 0,2 M 20 mmol molaritas garam: g 20 mmol (100 mL 100 mL) 10 1 M Garam yang térbentuk bersifat basa séhingga menggunakan rumus 10 5 pOH 5 pH 14 5 9 Jadi, pH larutan setelah dicampur adalah 9 (E). Silakan bertanya di kolom komentar apabila ada pembahasan yang kurang jelas. Delete Response Reply Unknown 1 Might 2017 at 12:25 Kalau yg sisa asam lemah dan garam kan harus pakai buffer mol garam nyá apakah harus dibági dengan volume overall Delete Replies Reply Akhmad Jazuli 1 Might 2017 at 13:58 Penentuan larutan penyanggabuffer tidak perlu dibagi volume total, karena: 1. Reply Delete Responses Akhmad Jazuli 1 Might 2017 at 15:15 Sama-sama Delete Responses Reply Reply Include comment Load more. Centang Notify me agar Andá mendapat pemberitahuan Iewat email bahwa komentar Anda sudah ditayangkan.
0 Comments
Leave a Reply. |
AuthorWrite something about yourself. No need to be fancy, just an overview. ArchivesCategories |
- Blog
- Can you buy office 2010 from microsoft
- Blog
- Ho to use better ds3 tool
- Scrabble blast free online
- Pc mac drive reader
- Sketchup 2017 free download for mac
- Ti 84 online help
- Www rick ross mp3
- Microsoft office packages for pc
- Amd ati mobility radeon hd 4250 graphics card driver
- How to download video from wowza streaming engine 4
- Canon pixma mg2120 manual download
- Best font management mac
- Blog
- Can you buy office 2010 from microsoft
- Blog
- Ho to use better ds3 tool
- Scrabble blast free online
- Pc mac drive reader
- Sketchup 2017 free download for mac
- Ti 84 online help
- Www rick ross mp3
- Microsoft office packages for pc
- Amd ati mobility radeon hd 4250 graphics card driver
- How to download video from wowza streaming engine 4
- Canon pixma mg2120 manual download
- Best font management mac
Search by typing & pressing enter

 RSS Feed
RSS Feed
